The Scientific Foundations of Human Genome Editing
76th Cellular, Tissue, and Gene Therapies Advisory Committee
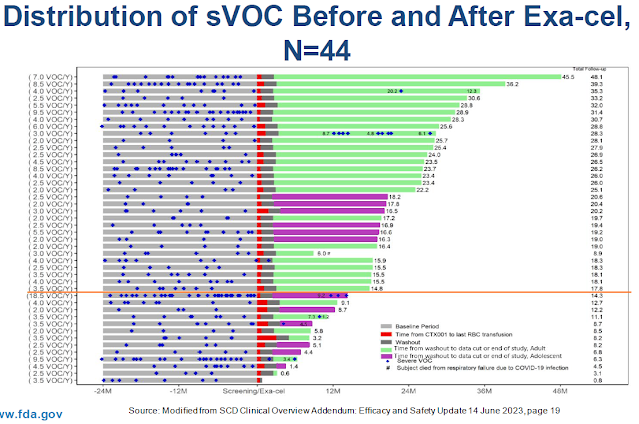
Clinical Assessment of Exa-cel
Panel Says That Innovative Sickle Cell Cure Is Safe Enough for Patients
El dimarts 31 vaig tenir ocasió d'assistir a una sessió històrica a la FDA. El consell assessor de teràpies cel·lulars, genètiques i de teixits debatia sobre una nova teràpia Exa-cel basada en CRISPR ex-vivo. Vull assenyalar en primer lloc que el nivell de trasparència de la FDA és realment impressionant. Tothom que vulgui pot assistir a la sessió online, hi havia més de 2000 persones connectades.
Exa-cel és una teràpia genètica desenvolupada per CRISPR Therapeutics conjuntament amb Vertex dirigida a l'anèmia de cèl·lules falciformes. Una malaltia que provoca oclusions vasculars, requereix múltiples transfusions, limita la qualitat de vida i escurça la vida.
Si teniu una bona estona podeu veure-ho a Youtube. És una sessió històrica perquè és la primera teràpia genètica que s'ha d'aprovar (previsiblement el 8 de desembre) basada en CRISPR. I la perspectiva d'aquest consell assessor era determinant pel que pot passar el desembre.
La sessió va tenir presentacions de fonaments de l'edició genètica, necessitats no cobertes, eficàcia clínica, seguretat no clínica, seguretat clínica i després debat. Un total de 7 hores de reunió!.
El resum del procés d'edició genètica: