The Right Price: A Value-Based Prescription for Drug Costs
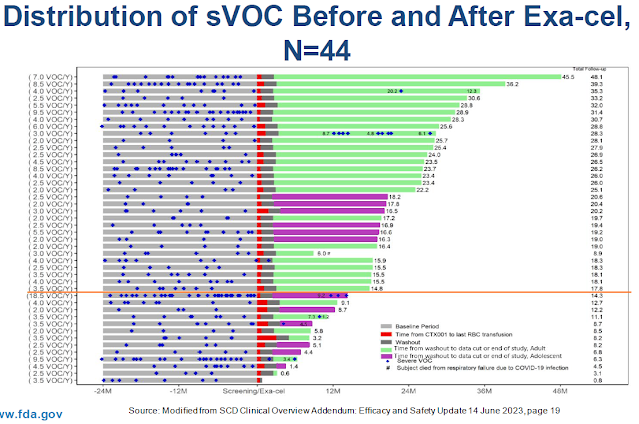
Ara que la FDA acaba d'aprovar la primera teràpia d'edició genètica mitjançant CRISPR per anèmia de cèl·lules falciformes, ja sabem el preu que ha decidit VERTEX, l'empresa comercialitzadora, 2,2 milions $. A Catalunya poden haver-hi unes 240 persones afectades i per tant l'impacte pressupostari del cost del tractament seria de més de 500 milions (si el preu final fos el que diuen ara). Aquesta és la dimensió del problema que s'acosta. La EMA l'aprovarà el mes de març proper.
Quin hauria de ser el preu adient d'un medicament?. Bona pregunta per un moment com aquest. Aquesta és precisament la qüestió que tracta un llibre de Peter Neumann et al. que he llegit recentment. Es tracta d'una obra per a tots els públics centrada als USA però que també va més enllà. L'índex ja dona una idea:
PART I. THE ECONOMICS OF PRESCRIPTION DRUGS
1.Introduction
2.The Prescription Drug Market
3.Proposed Solutions for Rising Drug Prices
4.Measuring the Value of Prescription Drugs
PART II. EXPERIENCES MEASURING A DRUG’S VALUE IN THE US AND ABROAD
5.Measuring Drug Value: Whose Job Is It Anyway?
6.Institute for Clinical and Economic Review
7.Other US Value Assessment Frameworks
8.Do Drugs for Special Populations Warrant Higher Prices?
PART III. GETTING TO VALUE-BASED PRICING FOR DRUGS
9.Improving Value Measurement
10.Aligning Prices With Value
11.The Path Forward
La tercera part m'ha interessat especialment perquè planteja qüestions sobre els QALYs que repetidament he explicat en aquest blog, i diu:
If QALYs were a person, they might receive a lot of hate mail. People complain that QALYs are not patient-focused, that they are used as rationing tools by health insurers, and that putting numbers on people’s health is dehumanizing. “The entire superstructure of the QALY methodology is built upon philosophical sand,” wrote one critic in 2019. As we have seen, the use of cost-per-QALY ratios by payers to inform drug coverage and pricing decisions attracts intense opposition in some quarters.
El racionament existeix però hipòcritament ningú en vol parlar, diu. I els QALYs tenen problemes però,
A philosopher and ethicist, Peter Singer, has observed (with apologies to Winston Churchill), QALYs may be the worst way to measure health, except for all of the others.
I així és. Som davant d'un llibre d'interès, especialment per a reguladors acabats d'arribar al càrrec i no tenen temps de llegir i s'enfronten al pànic escènic. És un llibre relativament curt que ajudarà a posar les idees en el context acurat.
PS. Tinc la impressió que cal superar la lògica del preu i anar cap una concepció diferent de contracte públic de subministrament de teràpies. Ho he explicat en altres ocasions i en canvi aquest llibre no ho reflecteix.
PS. Tinc la impressió que estem davant d'una teràpia amb gran potencial d'efecte crida, molt preocupant. Encara som a temps per regular-ho i evitar que passi com amb els peruans i el CAR-T. O es fa abans o ja serà massa tard i es farà malament.
PS. Aquí teniu un exemple de recerca en un àmbit on ja s'ha trobat la solució, i per tant és inapropiat invertir-hi. Ara bé, algú no se n'ha volgut adonar i uns altres hi estan abocant diners. Trobo a faltar informes sobre recerca fútil. Si voleu conèixer com s'ha arribat a la solució, ho trobareu aquí.
PS. Antic post sobre guerra injusta, per rellegir ara mateix.